NAMA : DIAN FERDINAN T
NIM : RRA1C114005
Buatlah
reaksi saponifikasi, nukleofil menyerang atau bereaksi dengan yang mana
sehingga membentuk sabun ?
Reaksi Sponifikasi/Penyabunan
Reaksi penyabunan merupakan reaksi hidrolisis
lemak/minyak dengan menggunakan basa kuat seperti NaOH atau KOH sehingga
menghasilkan gliserol dan garam asam lemak
atau sabun. Untuk menghasilkan
sabun yang keras digunakan NaOH, sedangkan untuk menghasilkan sabun yang lunak
atau sabun cair digunakan KOH. Perbedaan antara sabun keras dan lunak jika
dilihat dari kelarutannya dalam air yaitu sabun keras bersifat kurang larut
dalam air jika dibandingkan dengan sabun lunak. Reaksi penyabunan disebut juga
reaksi saponifikasi.
Reaksi Umum :
Mekanisme Reaksi :
RCOONa yang merupakan garam
dari natrium karboksilat dapat menjadi sabun apabila R (gugus alkil) yang
diikat merupakan gugus alkil yang besar seperti – C15H31
dan – C 16H33. Hal ini terjadi karena gugus alkil yang
besar memiliki sifat nonpolar, tidak seperti gugus alkil berantai pendek yang lebih
bersifat polar. Apabila sabun larut dalam air akan terbentuk ion RCOO- dengan
gugus R yang bersifat nonpolar dan COO- yang bersifat polar. Gugus R yang
terbentuk akan mengikat pengotor yang umumnya berbentuk lemak yang bersifat
nonpolar dan selanjutnya pada saat air dialirkan, air yang bersifat polar akan
menarik gugus nonpolar dari sabun dan kotoran sehingga kotoran tersebut lepas
dari tubuh kita. Karena sabun dibuat dari bahan baku alami yang berupa lemak,
limbahnya tidak berbahaya terhadap lingkungan karena mudah diuraikan oleh
mikroorganisme,
Contoh Reaksi Substitusi Nukleofilik (Reaksi Stereospesifikasi /
Reaksi Walden) yang lain dan mekanisme nya !
Reaksi
stereospesifik adalah reaksi dimana stereokimia reaktan sepenuhnya menentukan
stereokimia produk tanpa pilihan.
Reaksi stereoselektif adalah reaksi dimana terdapat
pilihan jalur, tapi stereoisomer produk terbentuk karena jalur reaksi
yang menjadi lebih menguntungkan atau disukai daripada jalur lain yang
tersedia.
Contoh:
Brominasi alkena merupakan salah satu contoh reaksi stereospesifik. Kedua karbon terikat ke salahs atu bromida kemudian bromida lain datang melalui bagian belakang menyerang salah satu karbon.
Brominasi alkena merupakan salah satu contoh reaksi stereospesifik. Kedua karbon terikat ke salahs atu bromida kemudian bromida lain datang melalui bagian belakang menyerang salah satu karbon.
Hidrogenasi alkena selalu stereoselektif. Jika
terdapat gugus metil atau tertbutil lebih disukai bentuk trans.
Penemuan Reaksi Substitusi
Nukleofilik
Tahun 1896, Walden melihat bahwa asam (-)-malat dapat
dirubah menjadi asam (+)-malat melalui tahapan reaksi kimia dengan pereaksi
a-kiral. Penemuan ini yang mengaitkan hubungan langsung putaran optik dengan
kekiralan dan perubahannya melalui alterasi kimia. Reaksi asam (-)-malat dengan
PCl5 menghasilkan asam (+)-klorosuksinat. Reaksi lebih lanjut dengan
perak oksida dalam air menghasilkan asam (+)-malat. Tahapan reaksi diawali
dengan asam (+) malat menghasilkan asam (-)-malat.
Contoh lain reaksi walden adalah reaksi antara (+)
asam klorosuksinat dengan KOH dan Ag2O.
a)
Reaksi substitusi nukleofilik
Pada reaksi
substitusi nukleofilik atom/ gugus yang diganti mempunyai elektronegativitas
lebih besar dari atom C, dan atom/gugus pengganti adalah suatu nukleofil, baik
nukleofil netral atau nukleofil yang bermuatan negatif.
a. Reaksi SN1
SN1/substitusi nukleofilik
unimolekuler mudah dikenali karena memiliki dua tahapan reaksi. Tahap pertama
merupakan tahap “perginya” (baca, putus/lepas) si gugus pergi dari suatu
senyawa/molekul yang nantinya akan digantikan oleh gugus datang. Gugus yang
pergi ini tidak sendiri, ia pergi dengan membawa pasangan elektron ikatan. Akibatnya
senyawa/molekul yang ditinggalkan mengalami kekurangan elektron. Dengan kata
lain senyawa mengalami ionisasi sehingga bermuatan positif dan memiliki
hibridisasi sp3 berbentuk segitiga planar/datar. Senyawa yang telah bermuatan
positif cenderung labil (mudah bereaksi) ketika berada dalam “mode” ini. Karena
itu gugus datang akan dengan mudah masuk dan membentuk ikatan dengan suatu
senyawa. Masuknya gugus datang dapat terjadi melalui dua arah yang berbeda,
karnanya produk hasil reaksi SN1 akan berupa rasemat/campuran
enantiomer/senyawa sama namun letak gugus datang dalam ruang 3D-nya berbeda.
Ada
analogi menarik perihal SN1, fenomenanya mirip-mirip dengan pasutri yang harus
melabuhkan kapal ditengah lautan, lalu berjalan berlawanan dengan damai karena
tidak adanya dukungan keadaan (cerai/pisah/terionisasi maksudnya). Disinilah
terbuka peluang bagi “calon-calon” gugus datang yang ingin mengisi kekosongan.
Alhasil, mudah bagi si calon untuk mengisi “kursi” yang ditinggalkan sang
mantan.
b. Reaksi
SN2
Berbeda
dengan SN1, reaksi SN2 (bimolekular) melibatkan dua gugus sekaligus selama
proses substitusi berlansung. Artinya reaksi akan sangat dipengaruhi oleh
kekuatan masing-masing gugus baik gugus datang maupun gugus pergi. Jika gugus
yang datang merupakan pendonor elektron yang lebih baik dari gugus yang akan
pergi, maka reaksi substitusi akan berlansung dengan mudah, sebaliknya jika
gugus pergi cenderung lebih baik dari gugus datang maka reaksi akan cenderung
lambat bahkan tidak berlansung sama sekali.
Jika produk
SN1 berupa rasemat maka produk SN2 berupa produk inversi (terbalik) yang
dikenal sebagai inversi Walden. “Fenomena” inversi terjadi sebagai akibat dari
adanya perubahan/pergantian letak gugus datang dan pergi sebelum dan sesudah
reaksi berlansung.
b)
Reaksi substitusi elektrofilik
Benzena
memiliki rumus molekul C6H6, dari rumus molekul tersebut benzena termasuk
golongan senyawa hidrokarbon tidak jenuh. Namun ternyata benzena mempunyai
sifat kimia yang berbeda dengan senyawa hidrokarbon tidak jenuh. Beberapa
perbedaan sifat benzena dengan senyawa hidrokarbon tidak jenuh adalah
diantaranya bahwa benzena tidak mengalami reaksi adisi melainkan mengalami
reaksi substitusi. Pada umumnya reaksi yang terjadi terhadap molekul benzena
adalah reaksi substitusi elektrofilik, hal ini disebabkan karena benzena
merupakan molekul yang kaya electron.
Ada 4 macam
reaksi substitusi elektrofilik terhadap senyawa aromatik,yaitu :
1)
Mekanisme Reaksi SN2
Mekanisme Reaksi SN2 hanya terjadi
pada alkil halida primer dan sekunder. Nukleofil yang menyerang adalah jenis
nukleofil yang kuat seperti -OH, -CN, CH3O-.
Serangan dilakukan dari belakang. Contoh reaksi mekanisme SN2 bromoetana dengan
ion hidroksida berikut ini :
2)
Mekanisme Reaksi SN1
Mekanisme Reaksi SN1 hanya terjadi
pada alkil halida tersier. Nukleofil yang dapat menyerang adalah nukleofil basa
yang sangat lemah seperti H2O, CH3CH2OH.
Terdiri dari 3 tahap reaksi.
Contohnya reaksi antara t-butil bromida dengan air.
Tahap 1:
Tahap 2 :
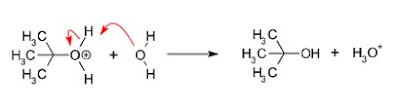
Tahap 3 :
1)
Mekanisme reaksi E1
Mekanisme reaksi E1 merupakan alternatif dari mekanisme reaksi SN1.
Karbokation dapat memberikan sebuah proton kepada suatu basa dalam reaksi
eliminasi.
Mekanisme reaksi E1 terdiri dari dua tahap. Perhatikan contoh berikut ini.
Tahap 1 :
Mekanisme reaksi E1 terdiri dari dua tahap. Perhatikan contoh berikut ini.
Tahap 1 :
Tahap 1 reaksi E1 berjalan lambat.
Tahap 2 :
Tahap 2 reaksi E1 berjalan cepat.


















Tidak ada komentar:
Posting Komentar